Abbasso il Colesterolo!
Facciamo Progressi!
di Leonardo De Luca
E’ meglio amare o essere amati?
Nessuna delle due se hai 600 di colesterolo!
(Woody Allen)
La frase di Woody Allen individua, con geniale sintesi, la corretta percezione nella cultura comune dell’impatto sulla vita quotidiana e sulla prognosi dell’ipercolesterolemia (un eccesso di colesterolo nel sangue), che in casi estremi sovrasta persino fondamentali domande filosofiche. Di fatto, e sinteticamente, l’ipercolesterolemia è la principale responsabile dell’aterosclerosi e quindi delle patologie cardiovascolari (CV) che continuano ad essere la principale causa di mortalità nel mondo occidentale. Ma procediamo con ordine.
Il colesterolo è una sostanza grassa necessaria al corretto funzionamento dell’organismo: partecipa infatti alla sintesi di alcuni ormoni e della vitamina D ed è un costituente delle membrane delle cellule. Prodotto dal fegato, può anche essere introdotto con la dieta: è contenuto, per esempio, nei cibi ricchi di grassi animali, come carne, burro, salumi, formaggi, tuorlo dell’uovo, fegato. Il trasporto del colesterolo attraverso il sangue è affidato a una classe particolare di particelle, quella delle lipoproteine. Esistono quattro tipi di lipoproteine, classificate in base alla densità, che è inversamente proporzionale alla quantità di colesterolo presente. Le più importanti per la prevenzione cardiovascolare sono:
- LDL, o lipoproteine a bassa densità: trasportano il colesterolo sintetizzato dal fegato alle cellule del corpo, comunemente definito ‘colesterolo cattivo’;
- HDL, o lipoproteine ad alta densità: rimuovono il colesterolo in eccesso dai diversi tessuti e lo trasportano nuovamente al fegato, che poi provvede a eliminarlo. Un eccesso di colesterolo HDL è quindi un fattore favorevole ed è pertanto denominato ‘colesterolo buono’.
La captazione delle LDL da parte delle cellule avviene ad opera di un recettore specifico (LDL-R), presente sulla superficie cellulare, che lega le LDL e le trasporta all’interno della cellula, con un processo chiamato endocitosi recettore-mediata. Quando le LDL sono presenti in concentrazioni eccessive, il loro accumulo nella parete arteriosa promuove la formazione e lo sviluppo dell’aterosclerosi dalla fase iniziali alle forme più severe, causa di angina, infarto, ictus ed altre patologie cardiovascolari.
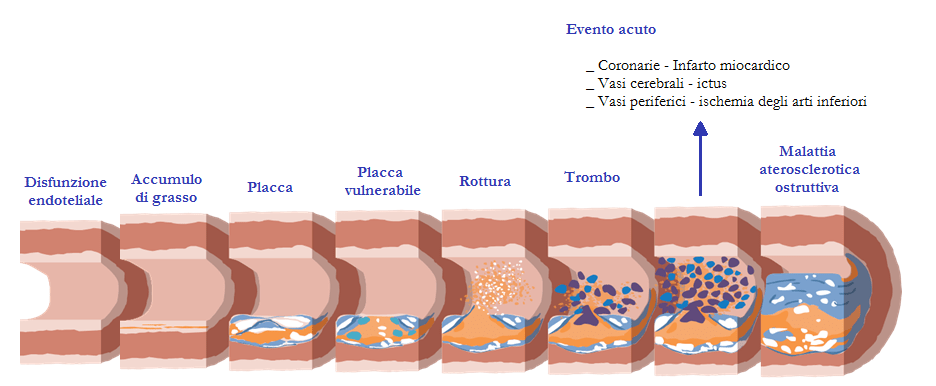
Di conseguenza l’ipercolesterolemia da LDL rappresenta uno dei maggiori fattori di rischio per le malattie cardiovascolari.
Ipercolesterolemia e rischio cardiovascolare
L’identificazione dell’ipercolesterolemia quale fattore di rischio cardiovascolare è il risultato di una lunga serie di studi epidemiologici che hanno messo in evidenza la correlazione tra colesterolemia ed eventi ischemici CV, in primo luogo l’infarto del miocardio e la mortalità CV, della quale l’infarto miocardico e l’ictus cerebrale costituiscono le cause più frequenti. Numerosi studi longitudinali – cioè studi che hanno tenuto sotto osservazione gli stessi individui per diversi anni – hanno chiaramente indicato che la correlazione tra colesterolemia e mortalità cardiovascolare è costantemente positiva lungo tutto l’intervallo dei valori della colesterolemia, senza che si possa individuare un valore soglia, al di sotto del quale il rischio si mantenga costantemente basso. Tale correlazione è di tipo curvilineare, cosicché al crescere della colesterolemia la mortalità da cardiopatia ischemica aumenta più rapidamente, in modo tale che un aumento della colesterolemia pari ad un punto percentuale corrisponde un aumento di quasi due punti percentuali della mortalità: rispetto a 200 mg/dl di colesterolemia, il tasso di mortalità è raddoppiato a 250 mg/dl e quadruplicato a 300 mg/dl. Inoltre da questi studi è emerso chiaramente che i vari fattori di rischio esaminati (principalmente ipertensione, fumo, diabete, obesità, familiarità per cardiopatia ischemica e bassi livelli di HDL) si potenziano a vicenda, per cui tanto più numerosi sono i fattori di rischio in un singolo individuo, tanto maggiore sarà la probabilità di morte per cause cardiovascolari.
A sostegno del ruolo causale della colesterolemia nella patologia cardiovascolare sopravvengono gli studi sperimentali (pur con i limiti del carattere sperimentale) e gli studi clinici. Gli studi sperimentali hanno accertato l’importanza delle LDL nella patogenesi dell’aterosclerosi, mentre gli studi clinici hanno dimostrato che la riduzione della colesterolemia si accompagna effettivamente ad una riduzione degli eventi cardiovascolari ischemici ed un aumento della sopravvivenza rispetto ai soggetti non trattati.
Tuttavia nella realtà clinica il discorso è più complesso. Non possiamo difatti facilmente prevedere i livelli di colesterolemia sulla base del colesterolo assunto per via esogena (con la dieta) in quanto esistono diversi metabolismi ed assorbimenti. Inoltre, a parità di colesterolemia, l’incidenza della mortalità per cardiopatia ischemica presenta notevoli differenze fra le diverse popolazioni. È stato quindi ipotizzato che la relazione tra dieta e colesterolo spieghi solo in parte gli effetti dell’introito di colesterolo con la dieta sulla mortalità coronarica. Infatti è probabile che ad un dato valore di colesterolemia totale corrispondano differenti livelli di LDL ossidate (le vere responsabili dell’aterosclerosi) e che differenze qualitative e quantitative nella composizione della dieta potrebbero avere notevole influenza sul grado di ossidazione delle LDL (es. le vitamine antiossidanti C, E e beta-carotene oppure i flavonoidi). La dieta mediterranea e quella giapponese, a basso contenuto di grassi saturi e ricche di antiossidanti e grassi insaturi, oltre ad un effetto diretto sui livelli delle LDL, potrebbero avere azioni favorevoli sia sull’ossidazione delle LDL che sulla trombogenesi.
Classificazioni dell’ipercolesterolemia ed ipercolesterolemia familiare
In base alle cause, le ipercolesterolemie possono essere distinte in primitive o secondarie. Le prime non risultano associate ad altre malattie che possono alterare il metabolismo lipidico, mentre le seconde sono causate da altre affezioni in grado di influenzare il metabolismo delle lipoproteine (ad es. cirrosi biliare primitiva, diabete mellito, sindrome nefrosica, uso prolungato di farmaci come i cortisonici e contraccettivi orali).
Tra le forme più comuni di ipercolesterolemie primitive vi è la ipercolesterolemia familiare (FH). L’FH è una patologia rara, ereditaria, associata ad elevati valori di colesterolo LDL che può portare all’insorgenza precoce di malattia cardiovascolare. L’accumulo di LDL nel sangue può verificarsi fin dalla giovane età ed espone i pazienti al rischio di aterosclerosi e al rischio cardiovascolare precoce. Infatti, i soggetti affetti da FH non riescono a metabolizzare correttamente il colesterolo endogeno, determinando un aumento dei livelli di colesterolo LDL, con conseguente ostruzione delle arterie e rischio di infarto, arresto cardiaco o ictus cerebrale. Nel complesso la FH non trattata comporta un incremento di 20 volte del rischio di infarto miocardico già prima dei 60 anni.
L’alterazione che si riscontra più frequentemente è a carico del gene che codifica per il recettore delle LDL. L’alterazione del gene provoca la formazione di recettori per le LDL malfunzionanti, ossia di recettori che non sono in grado di rimuovere il colesterolo LDL dal sangue. Esistono due forme principali di FH: la forma eterozigote e quella omozigote. Nella forma eterozigote è presente una copia normale del gene (quella derivante dal genitore sano), mentre l’altra (che proviene dal genitore affetto da FH) è alterata. Il recettore è quindi presente ma è prodotto in quantità insufficiente (50%). Nella forma omozigote entrambe le copie del gene sono alterate, e il recettore è del tutto assente o molto ridotto (da 0 a 25%). La forma eterozigote è la più comune (1/500 nati vivi) e presenta valori di colesterolemia che vanno da 220 mg/dl (di poco superiore alla norma) fino a circa 550 mg/dl. La forma omozigote è molto più grave, ma anche più rara (1/1.000.000 nati vivi) e le persone affette possono avere valori di colesterolemia di 550-1000 mg/dl, soprattutto sotto forma di LDL. Nel mondo si stimano 14-34 milioni di soggetti affetti da FH e, di queste, ogni anno circa 200.000 muoiono in seguito a problematiche cardiovascolari. In Italia si stimano dai 120 ai 250 mila soggetti con FH eterozigote.
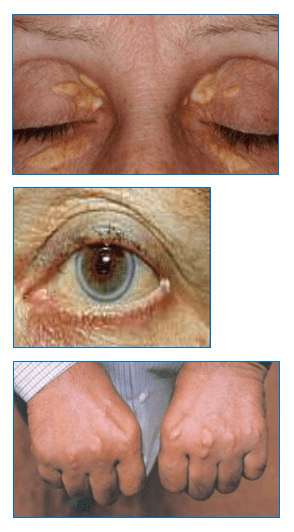
Un segno tipico è la frequente comparsa (dopo i 30-40 anni negli eterozigoti ed entro i primi 4 anni di vita negli omozigoti), di xantomi, cioè accumuli di grasso che si possono formare a livello dei tendini negli eterozigoti (xantomi tendinei) e a livello della cute dei gomiti e delle ginocchia negli omozigoti (xantomi cutanei). Altri segni spesso presenti negli eterozigoti sono gli xantelasmi (accumuli di grasso che si formano all’esterno dell’occhio) e l’arco corneale (piccola lunetta o anello grigio che si forma all’interno dell’occhio, alla periferia dell’iride).
La forma eterozigote può essere clinicamente silente ed essere riscontrata solo dopo un controllo casuale o non essere affatto riconosciuta. Dati dell’OMS suggeriscono che la FH è di gran lunga sotto-diagnosticata nella maggior parte dei Paesi. A testimonianza di ciò, anche la donna più osservata al mondo, la Monnalisa, presenta, ad un’analisi accurata, segni come xantomi e xantelasmi, suggestivi di ipercolesterolemia che meriterebbero ulteriori approfondimenti diagnostici.
 |
 |
 |
La diagnosi precoce è cruciale e il sospetto diagnostico andrebbe posto sulla base del quadro familiare e di criteri clinici. La prova diagnostica di FH può essere effettuata in laboratori specializzati a partire da un campione di sangue o di cute. Esiste anche la possibilità di una analisi genetica, analizzando direttamente il DNA dei pazienti, utile nelle forme incerte di FH: anche una analisi genetica negativa non esclude la presenza di FH. Allo scopo di definire una diagnosi clinica, sono raccomandati i criteri DLCN (Dutch Lipid Clinic Network), rappresentati in Figura 3.
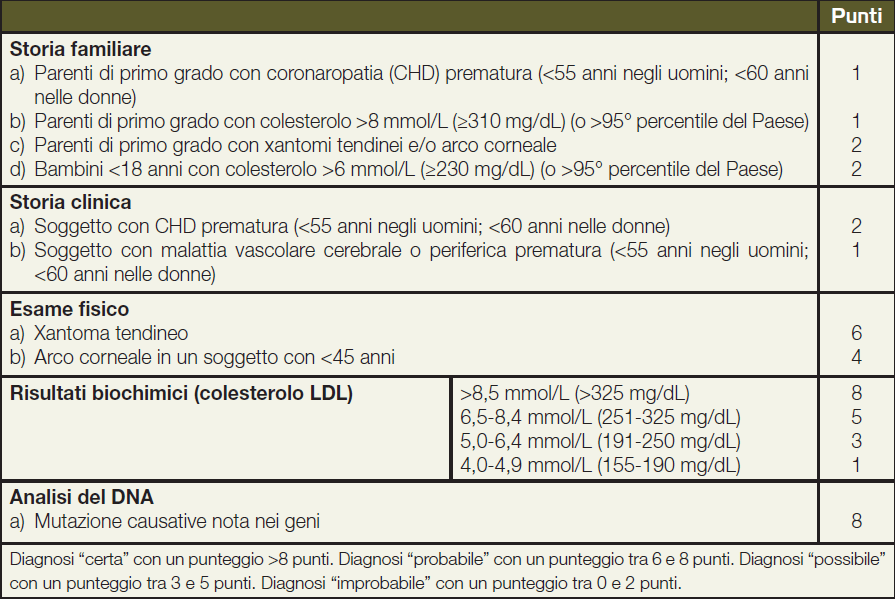
Terapia dell’ipercolesterolemia
La terapia dell’ipercolesterolemia prevede come intervento iniziale e imprescindibile una dieta a basso contenuto di grassi saturi (inferiore al 7% delle calorie totali) e in particolare di colesterolo (meno di 200 mg giornalieri). Solo nel caso in cui la dieta risultasse inefficace ad ottenere una soddisfacente riduzione della colesterolemia (come molto spesso accade) è prevista la contemporanea assunzione di farmaci, che debbono essere comunque affiancati alla dieta. Alla dieta deve essere affiancato uno stile di vita adeguato, che deve comprendere regolare attività fisica, interruzione del fumo e riduzione di peso. Ovviamente i target da raggiungere sono diversificati a seconda del profilo di rischio del paziente (ad es. nei soggetti ad elevato rischio CV come i diabetici o i pazienti con pregresso infarto il target attuale di LDL è inferiore a 70 mg/dl).
Le statine sono sicuramente i farmaci più efficaci nel ridurre i livelli plasmatici di colesterolo LDL. L’entità della riduzione della colesterolemia LDL che può essere raggiunta con la terapia a base di statine è strettamente dosaggio-dipendente e può superare il 40-50% di riduzione, agli alti dosaggi. Il meccanismo di azione di questi farmaci consiste nella inibizione competitiva dell’enzima regolatore della sintesi del colesterolo (HMGCoA-reduttasi), con azione di gran lunga prevalente a livello epatico (sede della sintesi endogena del colesterolo). L’inibizione dell’enzima causa una riduzione della concentrazione intracellulare di colesterolo; questa riduzione induce un aumento, sulla superficie cellulare, del numero dei recettori per le LDL. Il risultato è una maggiore captazione di LDL plasmatiche da parte degli epatociti, che provoca la riduzione della colesterolemia.
Gli effetti collaterali più importanti, anche se occorrenti in una bassa percentuale dei casi (<4%), comprendono l’aumento delle transaminasi (indice di danno epatico), di solito transitorio e comunque reversibile con la sospensione della terapia, e soprattutto l’aumento delle creatinchinasi (CPK), indice di danno muscolare, che è giunto in alcuni casi fino alla rabdomiolisi.
Da segnalare è poi l’ezetimibe, farmaco ipolipidemizzante da associare perlopiù alle statine, attivo per via orale, inibitore dell’assorbimento intestinale del colesterolo, primo di una nuova e interessante classe di farmaci. Il suo meccanismo di azione consiste nella inibizione di una proteina che trasporta il colesterolo dal lume intestinale nell’enterocita, modulando in tal modo l’assorbimento del colesterolo biliare e alimentare.
Gli anticorpi monoclonali anti-PCSK9
Nonostante la documentata efficacia delle statine, in numerosi pazienti – in particolare quelli caratterizzati da un alto rischio CV – i livelli ottimali di LDL-C, sono difficilmente raggiungibili con questa classe di farmaci. L’efficacia delle statine, inoltre, è limitata dal fatto che parallelamente all’aumento di espressione di LDL-R viene anche attivata come meccanismo di controllo negativo l’espressione di PCSK9 (proprotein convertase subtilisin/kexin 9). PCSK9 è una proteina appartenente alla famiglia delle proproteine convertasi che è in grado di legare LDL-R sia a livello intracellulare, sia sulla superficie della membrana plasmatica degli epatociti. Attraverso questo meccanismo, PCSK9 favorisce la degradazione di LD L-R in epatociti, fibroblasti e macrofagi. Mutazioni del gene PCSK9 che ne aumentano l’attività sono state riscontrate in pazienti con ipercolesterolemia autosomica dominante, mentre mutazioni con perdita di funzione sono state associate a bassi livelli di LDL e ridotto rischio CV, rivelando un ruolo importante di PCSK9 nella regolazione dei livelli di LDL. Queste osservazioni hanno stimolato un’intensa attività di ricerca su PCSK9 negli ultimi dieci anni, rendendo questa proteina uno dei più promettenti target per lo sviluppo di nuove terapie per il trattamento dell’ipercolesterolemia.
L’approccio più promettente per l’inibizione di PCSK9 è rappresentato dall’utilizzo degli anticorpi monoclonali. Tra i diversi anticorpi monoclonali diretti contro PCSK9, alirocumab ed evolocumab, anticorpi completamente umani somministrati per via sottocutanea una volta ogni due o quattro settimane, sono stati recentemente approvati dall’Agenzia Europea del farmaco. Numerosi studi pre-clinici e clinici sull’uomo hanno dimostrato l’efficacia degli anticorpi anti-PCSK9 sia in monoterapia che quando aggiunti alle statine e anche alla combinazione statine/ezetimibe, riducendo i livelli di LDL mediamente del 55-65% in soggetti con livelli basali di LDL compresi in un ampio range (70 e 200 mg/dl) e diversi profili clinici (dai pazienti con FH sia omozigote che eterozigote ai pazienti intolleranti alle statine). Recentemente questa classe di farmaci ha anche dimostrato una riduzione del volume della placca aterosclerotica dopo poche settimane di trattamento ed ha confermato un beneficio clinico nei pazienti ad alto rischio CV, riducendo, ad un follow-up pari a meno di tre anni, gli eventi clinici CV avversi (soprattutto le recidive di infarto miocardico e l’ictus ischemico) in maniera proporzionale alla riduzione di LDL (ed anche con livelli di LDL mai raggiunti con terapie farmacologiche). Ciò quindi conferma che così come esiste una correlazione lineare a crescere (maggiori i livelli di LDL, maggiore il rischio di eventi CV), così sussiste una correlazione negativa senza apparente soglia al ribasso (più abbasso i livelli di LDL, più riduco il rischio CV).
I dati a oggi disponibili indicano un adeguato profilo di sicurezza anche a lungo termine, con una bassa incidenza di effetti collaterali, peraltro simili tra il gruppo trattato con terapia standard e gruppo trattato con anticorpi monoclonali. Effetti collaterali più frequentemente descritti sono la comparsa di emicrania e, nel caso specifico della posologia sottocutanea, reazioni nel sito di somministrazione di natura per lo più lieve e transitoria. Un meta-analisi che ha valutato gli studi fino ad oggi disponibili, ha inoltre escluso che la somministrazione di anti-PCSK9 si associ con l’aumento di disordini neurocognitivi. Ciò è stato anche recentemente confermato da un largo studio condotto ad hoc che ha confermato la totale sicurezza ed assenza di disordini cognitivi associati ad anti-PCSK9, anche quando i livelli di colesterolo scendevano al di sotto di 30 mg/dl.
Tutto ciò conferma che l’attuale obiettivo terapeutico, soprattutto nei pazienti ad alto rischio CV è ridurre il più possibile i livelli di colesterolo, e più precisamente di LDL. In conclusione, il paradigma di prevenzione degli eventi CV può sintetizzarsi con tre sole parole: abbasso il colesterolo!
Tutto quel che non si mangia, fa bene alla salute.
Guido Ceronetti